SJM, 25/05/2026
HEREDITARIEDADE
O que é Hereditariedade?
A hereditariedade é o mecanismo biológico que explica por que os filhos se parecem com os pais, mas não são cópias idênticas deles. É, basicamente, a transmissão de características de uma geração para a outra.
Aqui está o resumo do que é essencial para o 9º ano:
1. Onde a informação fica guardada?
Dentro das nossas células existe um "manual de instruções" completo do nosso organismo: o DNA.
Genes: São pedaços específicos do DNA. Cada gene é uma receita para uma característica, como a cor dos olhos, o tipo de cabelo ou o formato da orelha.
Cromossomos: Para caber na célula, o DNA fica todo empacotado em estruturas chamadas cromossomos. Nós, humanos, temos 46 cromossomos na maioria das nossas células.
Genes: São pedaços específicos do DNA. Cada gene é uma receita para uma característica, como a cor dos olhos, o tipo de cabelo ou o formato da orelha.
Cromossomos: Para caber na célula, o DNA fica todo empacotado em estruturas chamadas cromossomos. Nós, humanos, temos 46 cromossomos na maioria das nossas células.
2. A receita vem em dose dupla
Nós recebemos metade das nossas instruções da mãe e metade do pai. Por isso, os nossos 46 cromossomos são organizados em 23 pares:
23 vieram no óvulo (mãe)
23 vieram no espermatozoide (pai)
Como os cromossomos estão em pares, os genes também estão. Cada versão de um gene que recebemos é chamada de alelo. Você tem dois alelos para cada característica: um materno e um paterno.
23 vieram no óvulo (mãe)
23 vieram no espermatozoide (pai)
3. Genótipo vs. Fenótipo
Essa dupla de conceitos é fundamental:
Genótipo: É o conjunto de genes que você carrega no seu DNA (a informação invisível a olho nu).
Fenótipo: É a característica física ou biológica que a gente realmente vê (o resultado).
O fenótipo não depende só dos genes; ele pode ser modificado pelo meio em que vivemos. A regra básica é:
Fenótipo = Genótipo + Ambiente
(Exemplo: Uma pessoa pode ter os genes para ser alta [genótipo], mas se tiver uma má nutrição na infância [ambiente], pode não crescer tanto quanto poderia [fenótipo]).
Genótipo: É o conjunto de genes que você carrega no seu DNA (a informação invisível a olho nu).
Fenótipo: É a característica física ou biológica que a gente realmente vê (o resultado).
Fenótipo = Genótipo + Ambiente
4. Alelos Dominantes e Recessivos
Na hora de definir como seremos, alguns alelos são mais "fortes" que outros:
Alelo Dominante: É aquele que consegue se manifestar mesmo se você herdar apenas uma cópia dele. Usamos uma letra maiúscula para representá-lo (ex: A).
Alelo Recessivo: É mais "tímido". Ele só consegue se manifestar e aparecer no fenótipo se você herdar duas cópias dele (uma do pai e uma da mãe). Se estiver junto com um dominante, ele fica escondido. Usamos letra minúscula (ex: a).
Por causa disso, a combinação dos alelos pode ser:
Homozigota (ou Pura): Quando os dois alelos são iguais (AA ou aa).
Heterozigota (ou Híbrida): Quando os dois alelos são diferentes (Aa). Nesse caso, quem manda no visual é o dominante (A).
SJM, 15/5/2026
A Distribuição Eletrônica
Alelo Dominante: É aquele que consegue se manifestar mesmo se você herdar apenas uma cópia dele. Usamos uma letra maiúscula para representá-lo (ex: A).
Alelo Recessivo: É mais "tímido". Ele só consegue se manifestar e aparecer no fenótipo se você herdar duas cópias dele (uma do pai e uma da mãe). Se estiver junto com um dominante, ele fica escondido. Usamos letra minúscula (ex: a).
Homozigota (ou Pura): Quando os dois alelos são iguais (AA ou aa).
Heterozigota (ou Híbrida): Quando os dois alelos são diferentes (Aa). Nesse caso, quem manda no visual é o dominante (A).
A Distribuição Eletrônica
A distribuição (ou configuração) eletrônica é a forma como os elétrons de um elemento químico se organizam ao redor do núcleo de um átomo. Com base no modelo atômico de Bohr, compreende-se que os elétrons ficam distribuídos em órbitas na eletrosfera.
Uma regra fundamental dessa organização é: quanto mais distante o elétron estiver do núcleo, maior será o seu nível de energia.
A distribuição (ou configuração) eletrônica é a forma como os elétrons de um elemento químico se organizam ao redor do núcleo de um átomo. Com base no modelo atômico de Bohr, compreende-se que os elétrons ficam distribuídos em órbitas na eletrosfera.
Uma regra fundamental dessa organização é: quanto mais distante o elétron estiver do núcleo, maior será o seu nível de energia.
Os Níveis de Energia (Camadas Eletrônicas)
A eletrosfera é dividida em até 7 camadas (ou níveis de energia), que correspondem aos 7 períodos da Tabela Periódica. Elas são representadas por letras maiúsculas e possuem um limite máximo de elétrons que conseguem suportar:
1º nível (Camada K): suporta até 2 elétrons
2º nível (Camada L): suporta até 8 elétrons
3º nível (Camada M): suporta até 18 elétrons
4º nível (Camada N): suporta até 32 elétrons
5º nível (Camada O): suporta até 32 elétrons
6º nível (Camada P): suporta até 18 elétrons
7º nível (Camada Q): suporta até 8 elétrons
A Camada de Valência: É a camada mais externa de um átomo (a última a receber elétrons). De acordo com a Regra do Octeto, os átomos tendem a buscar estabilidade química ficando com 8 elétrons nessa última camada.
A eletrosfera é dividida em até 7 camadas (ou níveis de energia), que correspondem aos 7 períodos da Tabela Periódica. Elas são representadas por letras maiúsculas e possuem um limite máximo de elétrons que conseguem suportar:
1º nível (Camada K): suporta até 2 elétrons
2º nível (Camada L): suporta até 8 elétrons
3º nível (Camada M): suporta até 18 elétrons
4º nível (Camada N): suporta até 32 elétrons
5º nível (Camada O): suporta até 32 elétrons
6º nível (Camada P): suporta até 18 elétrons
7º nível (Camada Q): suporta até 8 elétrons
A Camada de Valência: É a camada mais externa de um átomo (a última a receber elétrons). De acordo com a Regra do Octeto, os átomos tendem a buscar estabilidade química ficando com 8 elétrons nessa última camada.
Os Subníveis de Energia
Dentro de cada camada eletrônica, os elétrons se subdividem em subníveis energéticos, representados por letras minúsculas. Eles também possuem uma capacidade máxima:
Subnível s: comporta até 2 elétrons
Subnível p: comporta até 6 elétrons
Subnível d: comporta até 10 elétrons
Subnível f: comporta até 14 elétrons
Dentro de cada camada eletrônica, os elétrons se subdividem em subníveis energéticos, representados por letras minúsculas. Eles também possuem uma capacidade máxima:
Subnível s: comporta até 2 elétrons
Subnível p: comporta até 6 elétrons
Subnível d: comporta até 10 elétrons
Subnível f: comporta até 14 elétrons
O Diagrama de Linus Pauling
O químico estadunidense Linus Pauling mapeou a distribuição dos elétrons criando um esquema lógico de preenchimento. A grande sacada do Diagrama de Pauling é que os elétrons não preenchem as camadas de forma linear (uma após a outra de forma reta), mas sim em ordem crescente de energia através de linhas diagonais.
Seguindo as diagonais do diagrama, a ordem correta de preenchimento é:
1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d¹⁰ 4p⁶ 5s² 4d¹⁰ 5p⁶ 6s² 4f¹⁴ 5d¹⁰ 6p⁶ 7s² 5f¹⁴ 6d¹⁰ 7p⁶
Como ler cada termo (exemplo: 1s²):
1 (número à frente): indica o nível de energia (neste caso, a Camada K).
s (letra): indica o subnível energético.
² (número sobrescrito/expoente): indica a quantidade de elétrons ocupando aquele espaço.
O químico estadunidense Linus Pauling mapeou a distribuição dos elétrons criando um esquema lógico de preenchimento. A grande sacada do Diagrama de Pauling é que os elétrons não preenchem as camadas de forma linear (uma após a outra de forma reta), mas sim em ordem crescente de energia através de linhas diagonais.
Seguindo as diagonais do diagrama, a ordem correta de preenchimento é:
1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d¹⁰ 4p⁶ 5s² 4d¹⁰ 5p⁶ 6s² 4f¹⁴ 5d¹⁰ 6p⁶ 7s² 5f¹⁴ 6d¹⁰ 7p⁶
Como ler cada termo (exemplo: 1s²):
1 (número à frente): indica o nível de energia (neste caso, a Camada K).
s (letra): indica o subnível energético.
² (número sobrescrito/expoente): indica a quantidade de elétrons ocupando aquele espaço.
Exemplo Prático de Distribuição
Vamos distribuir os elétrons do átomo de Ferro (Fe), que possui Número Atômico 26 (Z = 26). Isso significa que temos 26 elétrons para alocar.
Seguindo as setas diagonais do Diagrama de Pauling, vamos preenchendo os limites e somando os "expoentes" até chegarmos a 26:
1s² (temos 2 elétrons)
2s² (temos 4 elétrons)
2p⁶ (temos 10 elétrons)
3s² (temos 12 elétrons)
3p⁶ (temos 18 elétrons)
4s² (temos 20 elétrons)
Agora faltam apenas 6 para 26. O próximo da fila é o subnível 3d, que cabe até 10 elétrons. Usamos apenas a quantidade necessária: 3d⁶.
Configuração Eletrônica Final:
1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d⁶
Resumo por Camadas:
Se agruparmos os elétrons de acordo com o seu número principal (1, 2, 3 e 4), teremos o resumo por camadas do Ferro:
K (nível 1): 2 elétrons
L (nível 2): 2 + 6 = 8 elétrons
M (nível 3): 2 + 6 + 6 = 14 elétrons
N (nível 4): 2 elétrons
Vamos distribuir os elétrons do átomo de Ferro (Fe), que possui Número Atômico 26 (Z = 26). Isso significa que temos 26 elétrons para alocar.
Seguindo as setas diagonais do Diagrama de Pauling, vamos preenchendo os limites e somando os "expoentes" até chegarmos a 26:
1s²(temos 2 elétrons)2s²(temos 4 elétrons)2p⁶(temos 10 elétrons)3s²(temos 12 elétrons)3p⁶(temos 18 elétrons)4s²(temos 20 elétrons)Agora faltam apenas 6 para 26. O próximo da fila é o subnível
3d, que cabe até 10 elétrons. Usamos apenas a quantidade necessária:3d⁶.
Configuração Eletrônica Final:
1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d⁶
Resumo por Camadas:
Se agruparmos os elétrons de acordo com o seu número principal (1, 2, 3 e 4), teremos o resumo por camadas do Ferro:
K (nível 1): 2 elétrons
L (nível 2): 2 + 6 = 8 elétrons
M (nível 3): 2 + 6 + 6 = 14 elétrons
N (nível 4): 2 elétrons
SJM, 27/04/2026
Modelo atômico
2) Diferencie isótopos, isótonos e isóbaros.
3) Diferencie um átomo isoeletrônico de íon.
4) Dado o átomo 3 H 1:
O número 3 representa o quê? __________
O número 1 representa o quê? __________
5) O que é molécula? Dê exemplos.
6) Um átomo de Hélio representado por 3 He 2 (com carga -1) tem quantos elétrons? Explique.
SJM, 14 de abril de 2026
Tabela Periódica
A Tabela Periódica organiza todos os elementos químicos conhecidos de acordo com suas propriedades e comportamentos.
1. Organização Geral
Ordem Crescente: Os elementos são dispostos em ordem crescente de número atômico (Z), que representa a quantidade de prótons no núcleo do átomo.
Períodos: São as 7 linhas horizontais. O número do período indica a quantidade de camadas eletrônicas que o átomo possui.
Grupos ou Famílias: São as 18 colunas verticais. Elementos do mesmo grupo possuem propriedades químicas semelhantes e, geralmente, o mesmo número de elétrons na camada de valência.
Ordem Crescente: Os elementos são dispostos em ordem crescente de número atômico (Z), que representa a quantidade de prótons no núcleo do átomo.
Períodos: São as 7 linhas horizontais. O número do período indica a quantidade de camadas eletrônicas que o átomo possui.
Grupos ou Famílias: São as 18 colunas verticais. Elementos do mesmo grupo possuem propriedades químicas semelhantes e, geralmente, o mesmo número de elétrons na camada de valência.
2. Principais Grupos (Famílias)
Grupo 1 (1A): Metais Alcalinos.
Grupo 2 (2A): Metais Alcalinotérreos.
Grupo 17 (7A): Halogênios.
Grupo 18 (8A): Gases Nobres (estáveis, raramente reagem com outros elementos).
Grupo 1 (1A): Metais Alcalinos.
Grupo 2 (2A): Metais Alcalinotérreos.
Grupo 17 (7A): Halogênios.
Grupo 18 (8A): Gases Nobres (estáveis, raramente reagem com outros elementos).
3. Classificação dos Elementos
Metais: Formam a maior parte da tabela. São bons condutores de calor e eletricidade, brilham e são maleáveis.
Não metais (Ametais): Não conduzem bem a eletricidade, são quebradiços no estado sólido e podem ser encontrados em diversos estados físicos.
Hidrogênio: Um elemento único que não se encaixa perfeitamente em nenhum grupo, apesar de estar posicionado acima dos metais alcalinos.
Metais: Formam a maior parte da tabela. São bons condutores de calor e eletricidade, brilham e são maleáveis.
Não metais (Ametais): Não conduzem bem a eletricidade, são quebradiços no estado sólido e podem ser encontrados em diversos estados físicos.
Hidrogênio: Um elemento único que não se encaixa perfeitamente em nenhum grupo, apesar de estar posicionado acima dos metais alcalinos.
4. A Identificação no Quadrado
Cada "quadradinho" da tabela traz informações essenciais:
Símbolo químico (Ex: H, O, Fe).
Número atômico (posicionado no topo).
Massa atômica (geralmente na base).
- Nome do elemento.
SJM, 30/3/2026 CIÊNCIAS
ÍONS
Os íons são átomos que perderam ou ganharam elétrons durante reações químicas. Como o átomo deixa de ser neutro (onde o número de prótons é igual ao de elétrons), ele passa a ter uma carga elétrica
1. Tipos de Íons
Cátion: É um íon com carga positiva. Ele se forma quando um átomo perde um ou mais elétrons.
Ânion: É um íon com carga negativa. Ele se forma quando um átomo ganha um ou mais elétrons.
Cátion: É um íon com carga positiva. Ele se forma quando um átomo perde um ou mais elétrons.
Ânion: É um íon com carga negativa. Ele se forma quando um átomo ganha um ou mais elétrons.
2. Representação Química
A carga do íon é indicada no lado superior direito do símbolo do elemento:
3. Por que isso acontece? (Regra do Octeto)
Os átomos buscam estabilidade eletrônica. Para a maioria dos elementos, isso significa ter 8 elétrons na camada de valência (a camada mais externa), assemelhando-se aos gases nobres.
SJM, 25/3/2026 CIÊNCIAS
ÁTOMOS E SUAS RELAÇÕES (ISÓTOPOS, ISÓBAROS E ISÓTONOS)
Para compreender as semelhanças atômicas, precisamos lembrar que um átomo é definido pelo seu número de prótons (Z), nêutrons (n) e sua massa (A), onde A = Z + n.
1. Isótopos (Mesmo número de Prótons)
São átomos de um mesmo elemento químico que possuem o mesmo número atômico (Z), mas diferem na quantidade de nêutrons e, consequentemente, no número de massa (A).
Característica: Possuem propriedades químicas idênticas.
Exemplos:
Hidrogênio 1-H-1 (Prótio)
Hidrogênio 2-H-1 (Deutério)
Hidrogênio 3-H-1 (Trítio)
2. Isóbaros (Mesma Massa)
São átomos de elementos químicos diferentes (possuem números atômicos Z diferentes) que apresentam o mesmo número de massa (A).
Característica: Possuem propriedades físicas e químicas diferentes, mas a massa atômica é igual.
Exemplo: Cálcio 40-Ca-20 e Argônio 40-Ar-18. (Ambos possuem massa 40).
3. Isótonos (Mesmo número de Nêutrons)
São átomos de elementos químicos diferentes que possuem o mesmo número de nêutrons (n). Para identificá-los, subtraímos o número atômico da massa (A - Z).
Exemplo: Berílio 9 Be 4 e Boro 10 B 5.
Berílio: 9 - 4 = 5 nêutrons.
Boro: 10 - 5 = 5 nêutrons.
Tabela de Consulta Rápida
| Termo | O que é igual? | Macete (Letra destaque) |
| Isótopos | Prótons (Z) | P de Prótons |
| Isóbaros | Massa (A) | A de Massa |
| Isótonos | Nêutrons (n) | N de Nêutrons |
São João de Meriti, 16 de março de 2026
Atomística (Ciências)
Estrutura da Matéria: Os Átomos (Resumo do livro Telaris)
A matéria é tudo o que tem massa e ocupa lugar no espaço. Segundo a abordagem da coleção Telaris, o átomo é a unidade fundamental para entender a constituição de tudo o que existe.
O Conceito de Átomo:
A palavra átomo tem origem grega e significa "indivisível". Embora hoje a ciência saiba que o átomo possui divisões, o nome foi mantido para designar a unidade básica da matéria.
A Evolução dos Modelos Atômicos Os cientistas criaram modelos para explicar a estrutura atômica ao longo do tempo:
Dalton: O átomo seria uma esfera maciça, neutra e indivisível (como uma bola de bilhar).
Thomson: Descobriu o elétron. O átomo seria uma esfera de carga positiva com elétrons negativos espalhados (como um pudim de passas).
Rutherford: Demonstrou que o átomo tem um núcleo pequeno e positivo, com elétrons girando em volta em um grande espaço vazio (modelo planetário).
Bohr: Aperfeiçoou o modelo anterior, sugerindo que os elétrons giram em camadas de energia específicas.
Partículas Subatômicas O átomo é formado por duas regiões principais:
No Núcleo (Centro):
Prótons: Partículas com carga elétrica positiva (+).
Nêutrons: Partículas sem carga elétrica (neutras), que estabilizam o núcleo.
Na Eletrosfera (Região Externa):
Elétrons: Partículas com carga elétrica negativa (-) que orbitam o núcleo.
Identificação dos Elementos
Número Atômico (Z): É a quantidade de prótons no núcleo. É o que define o elemento químico.
Número de Massa (A): É a soma de prótons e nêutrons no núcleo (A = Z + n).
SJM, 2/3/26
Reações Físicas e Químicas (CIências)
1. Transformações Físicas
Ocorrem quando a matéria altera sua forma ou estado físico, mas sua composição química permanece a mesma. Não há formação de novas substâncias.
Exemplos: Mudanças de estado (gelo derretendo), rasgar um papel, dissolver açúcar em água ou quebrar um vidro.
Características: Geralmente são reversíveis e a molécula original continua sendo a mesma.
2. Reações Químicas (Transformações Químicas)
Ocorrem quando as substâncias iniciais (reagentes) interagem e se transformam em novas substâncias (produtos) com propriedades diferentes. Há o rearranjo dos átomos.
Exemplos: Combustão (queima), oxidação (ferrugem), fotossíntese, digestão de alimentos e apodrecimento de frutas.
Evidências de uma Reação Química:
Mudança de cor.
Liberação de gás (efervescência).
Formação de um precipitado (sólido).
Alteração de temperatura (liberação ou absorção de calor).
Emissão de luz.
3. Representação das Reações
As reações são representadas por Equações Químicas:
Lei de Lavoisier (Lei da Conservação das Massas): "Na natureza, nada se cria, nada se perde, tudo se transforma". Isso significa que a massa total dos reagentes deve ser igual à massa total dos produtos.
SJM, 4/3/2026 Ciências
Exercícios:
1. Diferencie, do ponto de vista da composição da matéria, uma transformação física de uma transformação química. Dê um exemplo cotidiano para cada uma.
2. Durante um experimento, ao misturar vinagre com bicarbonato de sódio, observa-se uma intensa efervescência. Explique por que esse fenômeno é considerado uma reação química e identifique qual evidência visual confirma essa conclusão.
3. Enuncie a Lei de Lavoisier e explique a sua importância para o entendimento das reações químicas que ocorrem em sistemas fechados.
4. Analise o processo de oxidação (ferrugem) em um prego de ferro exposto à umidade. Por que não podemos dizer que se trata apenas de uma mudança de aparência (física)? Justifique sua resposta com base no conceito de reagentes e produtos.
5. A queima de uma folha de papel e a fragmentação (picadinho) dessa mesma folha resultam em fenômenos diferentes. Descreva o que ocorre com as moléculas do papel em cada um dos casos.
S.J.M 11 de março de 2026 (902
A Atomística ramo da Química que estuda a estrutura do átomo, suas partículas subatômicas e as semelhanças entre diferentes átomos.
Abaixo, apresento um resumo dos tópicos principais com esquemas visuais descritivos baseados no conteúdo:
1. Estrutura Básica do Átomo
O átomo é dividido em duas regiões principais:
Núcleo: Pequeno e denso, contém Prótons (positivos) e Nêutrons (sem carga, que estabilizam o núcleo).
Eletrosfera: Região vasta ao redor do núcleo onde os Elétrons (negativos) orbitam. É cerca de 10.000 a 100.000 vezes maior que o núcleo.
Esquema Visual:
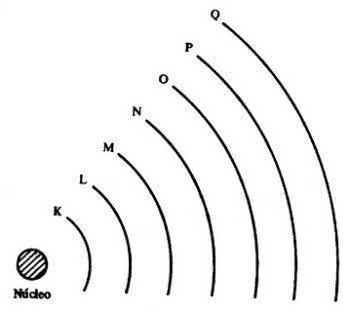
2. A Eletrosfera e Camadas de Energia
Refinado por Bohr, o modelo atual organiza a eletrosfera em 7 camadas orbitais (K, L, M, N, O, P, Q).
A camada K é a mais próxima do núcleo e tem menor energia.
A camada Q é a mais distante e possui maior energia.
3. Notações e Identidade Atômica
Para identificar um átomo, utilizamos:
Número Atômico (Z): Quantidade de prótons (é o "CPF" do elemento).
Número de Massa (A): Soma de prótons e nêutrons (A = Z + N).
4. Semelhanças Atômicas (Classificação)
O site destaca quatro tipos principais de relações entre átomos:
| Termo | O que é igual? | Dica de Memória |
| Isótopos | Mesmo número de Prótons (Z) | P de Prótons |
| Isóbaros | Mesmo número de Massa (A) | A de Massa |
| Isótonos | Mesmo número de Nêutrons (n) | N de Nêutrons |
| Isoeletrônicos | Mesma quantidade de Elétrons | - |
5. Íons (Átomos com Carga)
Quando um átomo perde ou ganha elétrons na eletrosfera:
Cátion: Perdeu elétrons (Carga Positiva).
Ânion: Ganhou elétrons (Carga Negativa).






Nenhum comentário:
Postar um comentário
Observação: somente um membro deste blog pode postar um comentário.